Через три месяца закончится 2021 год, а вместе с ним и возможность зарегистрировать медизделия по национальным правилам. Мы уже рассказывали о том, что можно сделать до начала следующего года и стоит ли надеяться на продление постановления 1416: теперь стоит отдельно остановиться на уже полученных регистрационных удостоверениях.
Если коротко: выданные до конца этого года РУ будут действовать ровно столько, сколько указано в сроках действия. Ситуация с ними никак не изменится.
Подробнее: От объединения национальных рынков членов ЕАЭС зависят только дальнейшие процессы регистрации. Если бессрочное РУ уже выдано, на оборот медизделий в РФ это не повлияет: проходить процедуры ЕАЭС нужно будет только в том случае, если производитель решит поставлять медизделия на рынок Армении, Беларуси, Киргизии или Казахстана. Внести изменения в РУ в ближайшие пять лет тоже можно по национальной схеме, не получая дополнительных документов формата ЕАЭС.
Недавно появилась информация о том, что для производителей, которые останутся с национальными РУ при полном переходе к рынку евразийского союза, могут исчезнуть налоговые льготы. По информации Минфина от НДС будут освобождены только медизделия, зарегистрированные по союзным правилам и медизделия, получившие национальное РУ до конца 2021 года.
Вот как это выглядит на конкретном примере:
Представим производителя Х, получившего национальное РУ на фонендоскопы в 2018 году. По этому РУ он может выпускать медизделия в обращение только на российской территории. Все, что будет происходить с фонендоскопами в ближайшее время, регулируется на двух уровнях: регламентами Евразийской Экономической Комиссии и законодательными актами членов ЕАЭС — в том числе России. Национальные правила РУ не менялись; более того, в недавно принятом ЕЭК распоряжении мы видим следующее:
Медицинское изделие, зарегистрированное в порядке, предусмотренном законодательством государства-члена ЕАЭС, выпускается в обращение на территории этого государства-члена до окончания срока документов, подтверждающих факт его регистрации.
То есть, если РУ бессрочное, на территории РФ оно будет действовать бессрочно — и в 2022, и в 2029, по крайней мере исходя из нынешней ситуации.
А теперь вопрос: есть ли в примере с производителем Х подводные камни?
Во-первых, его точно не касается следующий абзац из того же распоряжения (“Медицинское изделие, зарегистрированное по законодательству государства-члена, <…> может быть перерегистрировано до 31 декабря 2026 года”): в России — в отличие от, например, Беларуси — не существует процедуры перерегистрации. Впрочем, на эту дату придется ориентироваться в случае, если производитель будет вносить изменения в регистрационные документы: это можно будет сделать только до 31 декабря 2026.
И, конечно, чтобы расширить поставки фонендоскопов до территории всего ЕАЭС, производитель должен будет зарегистрировать их по союзным правилам: с национальным РУ он может выйти только на российский рынок. С НДС все немного сложнее: отчетливый ответ насчет налогообложения можно будет дать только после дальнейших распоряжений Минфина.
Сроки наглядно:
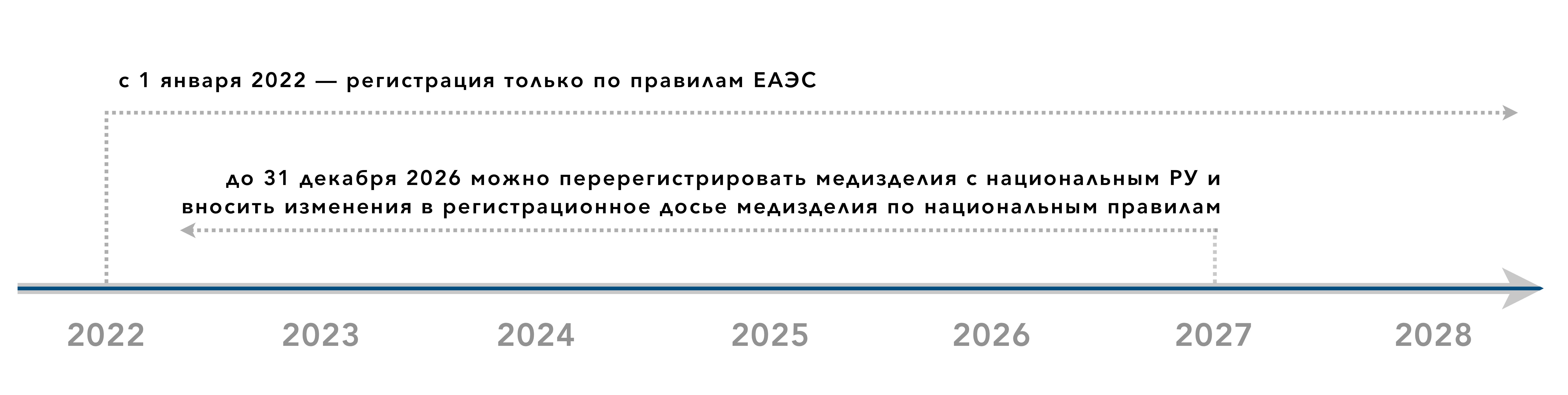
Полезные ссылки:
https://docs.eaeunion.org/docs/ru-ru/01528728/err_12032021_28 Распоряжение ЕЭК о сроках регистрации медизделий и внесении изменений в РУ (вступило в силу в марте 2021 года)
https://www.garant.ru/news/1402755 Новости Минфина насчет налоговых льгот




