Со времени создания Евразийского Экономического союза в 2014 году только в сфере здравоохранения принято более трехсот решений, так или иначе влияющих на оборот лекарств и медизделий внутри страны. Из последнего — 30 декабря 2021 года были внесены изменения в Соглашение о единых принципах и правилах обращения медицинских изделий: теперь внести изменения в срочные РУ, оформленные по национальной схеме, можно до 31 декабря 2026 года; переоформить их можно в те же сроки*.
Такие темпы принятия решений создают сложности для тех, кто в этих решениях пытается разобраться — производителей, дистрибьюторов и даже экспертов. Поэтому мы подготовили подробный навигатор по основным законодательным актам, актуальным на конец января 2022 года.
Медицинские изделия
Действующие документы — решения совета и коллегии ЕЭК, рекомендации и реестры — собраны в этой таблице (прокрутите вниз). Акты ЕЭК, касающиеся обращения медизделий, представлены здесь и вовремя обновляются, а гиперссылки ведут на pdf-файлы в удобном формате. Разберёмся с основными из списка.
В этом году регистрация медизделий, вроде бы, окончательно переведена в формат ЕАЭС: это значит, что подать заявление на регистрацию теперь можно только по союзному протоколу, который предусматривает другие испытания и расширенный набор документов для досье.
При подаче досье заявитель проходит четыре основных этапа: предварительная работа (определение вида и класса риска МИ), испытания (технические и клинические), выбор государства-референта и доработка документов и эскпертиза производства.
Где найти полный перечень документов для регистрации в ЕАЭС?
На страницах 46-53 решения Совета ЕЭК № 46 перечислены все документы, необходимые для регистрации, и форма справки. Мы рекомендуем руководствоваться именно этим перечнем и обращать внимание на примечания к каждому пункту: там прописано, кем должен заверяться каждый документ и перечислены формальные требования к документам. Содержательные требования изложены в недавно принятой Рекомендации ЕЭК № 29: там, например, регламентируется размер электронных файлов досье (не более 100 Мб на файл) и алгоритм проведения исследований. Для удобства мы разместим его в примечаниях (см. ниже).
Как определить класс риска медизделия?
Он определяется по Решению Коллегии ЕЭК № 173, где описаны все критерии по классам риска, в т.ч. для медизделий для диагностики in vitro. В приложении (с. 22 и далее) можно найти специальный алгоритм для классификации.
Как проводятся испытания?
Клинические испытания регулируются решением Совета ЕЭК № 29: в пункте VI описаны требования к проведению испытаний, список необходимых документов, пункты VII и VIII посвящены исследованиям медизделий для диагностики in vitro; в первом приложении есть готовый шаблон заявления, а в остальных перечислены требования к содержанию брошюры исследователя, техфайлу и программе испытаний для разных видов МИ. Там же можно найти готовые формы отчёта для заполнения.
Решение Совета ЕЭК № 28 регулирует технические испытания медизделий и форму отчета и протокола: она представлена в приложении к документу.
Кроме того, на отдельной странице собраны ссылки на все справочники и классификаторы, актуальные для предварительной работы по регистрации. Во всех вопросах, связанных с номенклатурой, классификацией и бюрократическими формальностями при оформлении досье, мы рекомендуем опираться именно на этот перечень. Если у вас возникнут затруднения или конкретные вопросы — мы будем рады ответить на них по почте regmed@regmed.biz
Примечания
*Подробнее — тут: Протокол о внесении изменения в Соглашение о единых принципах и правилах обращения медицинских изделий (изделий медицинского назначения и медицинской техники) в рамках Евразийского экономического союза от 23 декабря 2014 года (подписан в г. Москве 30.12.20216 вступит в силу 30 января 2022 г.)
** Алгоритм:
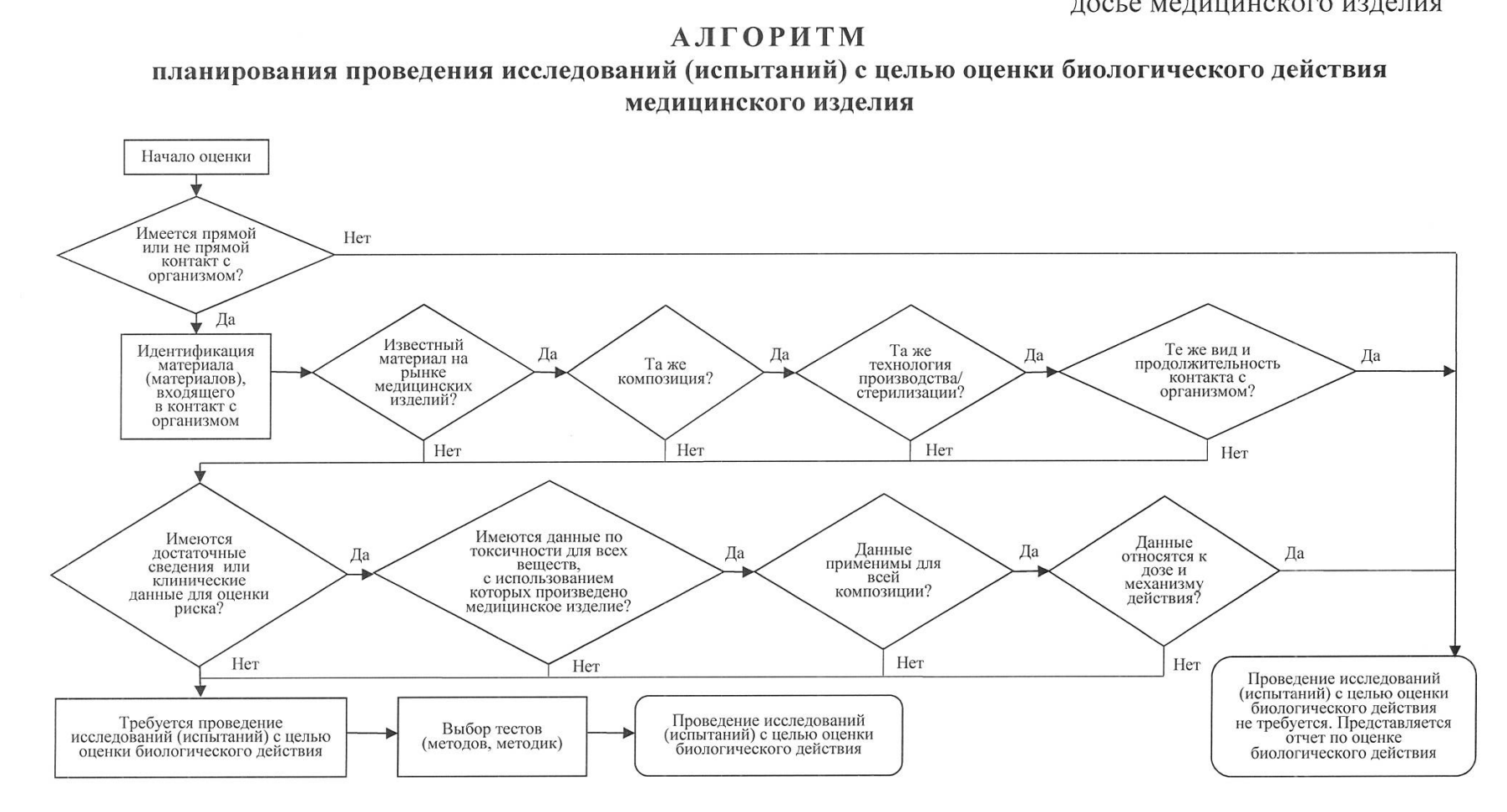
(Источник: Приложение к Методическим рекомендациям по содержанию и структуре регистрационного досье медицинского изделия. с. 21. Онлайн-доступ: https://docs.eaeunion.org/docs/ru-ru/01423420/clcr_11102019_29)